Бруцеллезный артрит
Инфекционный специфический артрит, одно из частых проявлений бруцеллеза.
Возбудитель
Наиболее часто инфекцию у собак вызывает B. canis, к которой невосприимчивы сельскохозяйственные животные. Этиологическим агентом бывают также B. abortus, B. melitensis и B. suis.
Эпизоотология
Бруцеллез, вызываемый видом Brucella canis, регистрируется даже в тех странах, где бруцеллез других видов животных не встречается (Великобритания, Германия, Чехия, Словакия, Япония). В РФ Вг. canis впервые зарегистрирована в 1994 году в Волгоградской области.
Пути передачи
Возбудитель Brucella canis выделяется с мочой, спермой, выделениями из матки, с фекалиями, молоком, слюной. Brucella canis может сохраняться в сперме кобелей до нескольких месяцев. Опасность представляют не только зараженные бруцеллезом собаки, но и щенки от них.
Суки в период беременности более восприимчивы к бруцеллезу.
Переболевшие животные остаются носителями на протяжении от нескольких месяцев до нескольких лет и приобретают пожизненный иммунитет.
Клиническая картина
Инкубационный период – 2-3 недели.
- часто протекает бессимптомно (возможна продолжительная, до двух лет и более, бактериемия без лихорадки).
- полилимфаденопатия
- артриты. Поражаются обычно крупные суставы, при остром и подостром течении наблюдаются их опухание, болезненность, повышение температуры кожных покровов сустава, иногда — покраснение кожи и выпот, нарушение функции конечности. При хроническом течении возможно поражение периартикулярных тканей, мышц и подкожной клетчатки, в результате чего возникают бурситы, тендовагиниты, фиброзиты, миозиты.
- орхиты, простатиты и эпидидимиты
- аборты (частично разложившиеся плоды на 45-55-й день беременности), мертворожденные приплоды, в дальнейшем — хронические эндометриты. Может наблюдаться ранняя эмбриональная смерть, которая выглядит как бесплодие суки.
- зараженные щенки рождаются мертвыми или слабыми, а у выживших сильно увеличены лимфатические узлы.
- иногда инфекция связана с остеомиелитом, дискоспондилитом и рецидивирующим увеитом
Особенности диагностики
- Рентгенологических изменений при остром и подостром течении в суставах обычно не определяется. На рентгенограмме при хроническом артрите можно отметить костно-хрящевую деструкцию вплоть до анкилоза.
- Цитологическое исследование синовии: серозный, стерильный выпот.
- Серологические тесты: РА (1:200 и выше), РСК (1:20 и выше). Агглютинины в крови появляются в зависимости от способа заражения в сроки от 3-14 до 20 дней. Нарастание титра агглютинации в среднем происходит до 20-30-го дня после появления патологического титра. Щенки, родившиеся от больных матерей, в первые 2-3 мес имеют РА в низких титрах. С помощью РСК определяется большее количество положительно реагирующих собак, и реакция удерживается длительнее. При естественном течении болезни чаще встречаются животные с различной длительностью заболевания, поэтому комплексное использование РА и РСК позволит выявить больше больных.
- ПЦР синовии, патматериала
- Посев на кровяных культурах
Лечение
Являясь факультативными внутриклеточными паразитами, бруцеллы мало чувствительны к традиционной антибиотикотерапии, поэтому лечение считается сложным и малорезультативным, зачастую позволяя лишь снизить остроту заболевания. Лечение МОЖЕТ БЫТЬ эффективно, если оно начато не позже 6-ти месяцев после заражения! Антибиотикотерапия наиболее эффективна при остросептической форме. При хронической форме течения основное значение имеет вакцинотерапия.
- ЛС выбора применяются не менее 1,5 месяцев: Доксицилин (12,5 мг/кг, 2 раза в день орально) и стрептомицин 20 мг/кг/сут в/м 2 раза в день в течение 15 дней. Затем – доксициклин и рифампицин по10-20мг/кг/сут внутрь в 2 приёма в течение оставшихся 30 дней лечения.
- Альтернативные ЛС применяются также не менее 1,5 месяцев: Ко-тримоксазол по 10-20мг/кг/сут внутрь 2р/д и рифампицин внутрь по 10-20мг/кг/сут
Возможно повторение курса лечения.
Распространенные ошибки лечения
- Проведение коротких (менее 1,5 мес) или прерывистых курсов антибиотикотерапии.
- Проведение монотерапии.
- Проведение антибактериальной терапии при латентных формах.
Источники
1. V. Brinkmann, «Neutrophil Extracellular Traps in the Second Decade», J. Innate Immun., т. 10, вып. 5–6, сс. 414–421, 2018.
2. B. G. Yipp и P. Kubes, «NETosis: how vital is it?», Blood, т. 122, вып. 16, сс. 2784–2794, окт. 2013.
3. T. A. Fuchs, A. Brill, и D. D. Wagner, «Neutrophil Extracellular Trap (NET) Impact on Deep Vein Thrombosis», Arterioscler. Thromb. Vasc. Biol., т. 32, вып. 8, сс. 1777–1783, авг. 2012.
4. J. Geddings и N. Mackman, «New players in haemostasis and thrombosis», Thromb. Haemost., т. 111, вып. 04, сс. 570–574, 2014.
5. M. Dwyer и др., «Cystic fibrosis sputum DNA has NETosis characteristics and neutrophil extracellular trap release is regulated by macrophage migration-inhibitory factor», J. Innate Immun., т. 6, вып. 6, сс. 765–779, 2014.
6. V. Marcos и др., «Free DNA in cystic fibrosis airway fluids correlates with airflow obstruction», Mediators Inflamm., т. 2015, с. 408935, 2015.
7. S. B. Coffelt, M. D. Wellenstein, и K. E. de Visser, «Neutrophils in cancer: neutral no more», Nat. Rev. Cancer, т. 16, вып. 7, сс. 431–446, 2016.
8. Park J. et al. Cancer cells induce metastasis-supporting neutrophil extracellular DNA traps //Science translational medicine. – 2016. – Т. 8. – №. 361. – С. 361ra138-361ra138.
Лечение дисфункции нейтрофилов
При врожденных нарушениях функции нейтрофилов редко возможно специфическое лечение. Однако диагностика функциональных нарушений нейтрофилов позволяет врачу предположить наличие бактериальных инфекций и заранее планировать медикаментозное лечение этих осложнений. При некоторых врожденных нарушениях, таких как синдром мраморных колли, помогает трансплантация костного мозга, но она производилась только во время научных исследований. В клинических условиях пересадка костного мозга непрактична, так как требуются значительная гистосовместимость и соответствие группы крови, пациентов нужно готовить к трансплантации путем облучения всего организма и химиотерапии, и трудно бывает бороться с бактериальной инфекцией во время приживления трансплантата. Из-за указанных соображений пересадка костного мозга считается сложной и дорогой.
Врачу лучше всего удается справиться с приобретенной дисфункцией нейтрофилов путем устранения или борьбы с основным заболеванием. Данный метод состоит в лечении соответствующими антибиотиками при бактериальной пиодермии путем четкого контроля введения инсулина при диабете и регулировании фосфора алиментарных нарушениях у животных.
Что такое лимфома
Это один из видов рака. Коварство этого недуга заключается в длительном бессимптомном течении. Зачастую владелец животного выявляет новообразования, когда их уже не вылечить. Опухоль поражает лимфатическую систему, которая является важным звеном в обменных процессах. Эта патология часто диагностируется у собак разных пород. Чаще всего она встречается:
у бульдогов;
сенбернаров;
эрдельтерьеров;
скотчтерьеров;
немецких овчарок;
боксеров;
лабрадоров;
и некоторых других.
Заболеваемость зависит от возраста, наиболее болезни подвержены животные шести-девяти лет. Обычный анализ крови помогает выявить этот недуг. На наличие патологии указывает увеличение общего количества лейкоцитов, в том числе у собаки повышены и сегментоядерные нейтрофилы. Выраженный лейкоцитоз наблюдается при гематологических и онкологических патологиях. Безусловно, одного лабораторного исследования недостаточно, чтобы выставить окончательный диагноз, так как у любого заболевания имеются свои характерные симптомы
Важно помнить, что незначительное повышение белых кровяных телец возникает и при физиологических состояниях – стресс, физическая нагрузка, беременность и лактация
Лимфома: причины, стадии и виды
Выделяют следующие причины возникновения болезни:
инфекционные;
генетические;
иммунологические;
негативное влияние окружающей среды;
отравления токсинами и пестицидами;
слабый иммунитет;
длительный прием антибактериальных средств.
Встречается несколько стадий недуга:
поражается один лимфоузел;
в процесс вовлекается несколько лимфатических узлов;
в организме происходит мутация узлов и их увеличение в размерах;
разрушается печень и селезенка;
в патологический процесс вовлекается нервная система, костный мозг и иные важные органы.
Существуют следующие виды заболевания и характерные для них симптомы:
- Медиастинальная – гиперкальциемия, увеличение лимфоузлов средостения.
- Экстранодальная – поражение конкретного органа: сердца, глаза, костного мозга, носовой полости, ЦНС, мочевого пузыря.
- Алиментарная или желудочно-кишечная – увеличение брюшины, кишечное расстройство, рвота, потеря массы тела. Поражение селезенки и печени.
- Кожная – воспаление лимфатических узлов.
- Многоцентровая – возникновение периферической лимфаденопатии.
Доказано, что менее всего подвержены раковым болезням стерилизованные и кастрированные домашние питомцы. Кроме того, их легче вылечить и процент усвояемости медикаментов у них выше.
Роль NETs в тромбозе
Хотя патогенез артериального и венозного тромбоза различен, в обоих этих процессах принимают участие NETs. При венозном тромбозе активированный эндотелий высвобождает фактор фон Виллебранда и P-селектин, которые привлекают тромбоциты и нейтрофилы. Во время активации тромбоциты индуцируют нейтрофилы, и те высвобождают внеклеточные ловушки, которые становятся каркасом для построения тромба и адгезии тромбоцитов. NETs способствует расщеплению ингибитора тканевого фактора и стимуляции Ха фактора .
NETs также играют значимую роль в образовании атеросклеротических бляшек, которые могут привести к артериальному тромбозу. При контакте нейтрофилов с кристаллами холестерина может спонтанно запускаться нетоз, который приводит к задержке тромбоцитов, активации коагуляции и образованию артериальных тромбов .
Сегментоядерные и палочкоядерные нейтрофилы
В крови животного присутствуют как зрелые клетки сегментоядерные, так и юные палочкоядерные. Обнаружение в крови большого количества палочкоядерных нейтрофилов означает, что организм вяло реагирует на болезнетворные и физиологические раздражители внешней среды. А при увеличении сегментарных подозревают онкологию, различные инфекции, почечную и печеночную недостаточность, воспалительные процессы.
Кроме того, их концентрация повышается при стрессе у собаки и после психоэмоционального возбуждения. Преобладание нейтрофилов сегментоядерных означает сдвиг лейкоцитарной формулы вправо. Из хранилища, находящегося в костном мозге, в кровоток выпускается большое количество зрелых кровяных клеток. В результате этого в циркулирующей крови снижается перемещение нейтрофилов в ткани.
Особенности нейтрофильной фазы воспалительных процессов
Для того чтобы понимать все особенности нейтрофильной фазы воспалительных процессов, очень желательно иметь ветеринарное или медицинское образование, но мы постараемся описать важную роль этих клеток более простыми и понятными словами.
Итак, именно нейтрофилы первыми устремляются в центр очага будущего воспаления (их, кстати, впоследствии сменяют моноциты). Также нужно упомянуть, что моноциты и другие макрофаги ориентируются на предварительно выброшенные нейтрофилами хемокины.
Что касается самих нейтрофилов, то в норме их концентрация в крови небольшая. Их выброс из красного костного мозга происходит после появления в крови маркеров воспаления. Основной задачей клеток при этом является адгезия к стенкам сосудов у места воспалительного процесса, проникновении через стенки сосудов (что обеспечивает гистамин, увеличивающий проницаемость последних). Далее они образуют основу лейкоцитарного вала (визуально это – красная линия воспаления). После этого наступает черед фагоцитоза и выброса лизирующих ферментов.
Наиболее сложным для нейтрофилов моментом является приближение к стенкам сосуда, «размазывание» по ней и проникновение в межклеточное пространство. Скорость этого процесса сравнительно невелика, так как лишь через два часа после момента проникновения (точнее, с момента обнаружения антигена лимфоцитами) к очагу воспаления прибывают первые нейтрофилы. Пиковая их концентрация создается примерно через 12 часов.
Бактериальный фон кожи у собак: резидентные и транзиторные микроорганизмы
Со здоровой кожи собак можно высеять значительный спектр различных так называемых нормальных обитателей кожи. Их классификация предполагает такие понятия, как резидентные и транзиторные бактерии. Подобное разделение понятий вызвано способностью к размножению тех или иных бактериальных организмов.
К резидентным относят бактерии, которые способны к размножению на поверхности кожи собак, – бактерии Micrococcus; коагулазонегативные стафилококки, особенно Staphylococcus epidermidis и Staphylococcus xylosus; α-гемолитические стрептококки; бактерии Clostridium, Propionibacterium acnes; бактерии Acinetobacter, а также разнообразные грамотрицательные аэробные бактерии и иные микроорганизмы.
К транзиторным бактериям, которые не обладают способностью к размножению на поверхности здоровой кожи собак, относятся Escherichia coli, Proteus mirabilis, бактерии вида Corynebacterium, Bacillus, Pseudomonas, другие бактерии.
Основным патогеном, который наиболее часто вызывает бактериальное воспаление кожи у собак, является Staphylococcus Pseudointermedius. Существуют различные вариации штаммов этих бактерий. Одни из них относятся к резидентной, а другие к транзиторной флоре.
Изучение свойств Staphylococcus Pseudointermedius позволило исследователям ответить на вопрос, почему именно эти микробные организмы наиболее часто являются причиной воспаления кожи у собак. В связи с этим было обнаружено, что стафилококки обладают способностью к выраженной адгезии с поверхностью кератиноцитов, и эти бактерии воздействуют на иммунную систему как суперантигены.При этом считается, что Staphylococcus Pseudointermedius не обладает высокой патогенностью и лишь вызывает вторичные инфекции.
Основные причины развития бактериального воспаления кожи у собак
В качестве предрасполагающих факторов, вызывающих развитие бактериального поражения дермы собак, рассматривают некоторые кожные, метаболические, иммунные нарушения, а также первичные паразитарные и грибковые инфекции. В связи с этим выделяют ряд причин, которые (собственно) и приводят к развитию вторичного бактериального процесса: себорейные нарушения, аденит сальных желез, фолликулярные дисплазии; гипотиреоидизм, гиперадренокортицизм; первичные и вторичные иммунодефициты, аллергии; демодекоз, дерматофитии.
Особенный интерес представляют иммунные нарушения, которые во многом являются ключевыми в развитии бактериальной инфекции.
Основные группы нарушений, формирующих пиодермию.
Чаще всего формируются вторичные иммунодефицитные состояния, возникающие в целом ряде случаев: на фоне применения иммуносупрессивных средств из-за перенесенного стресса или наличия заболеваний эндокринной системы, или прочих причин. Однако для собак актуальными являются также первичные иммунодефициты, обусловленные генетическими предпосылками. Они могут соотноситься с конкретными породами собак, например нарушение процессов биоцидности нейтрофилов у добермана-пинчера, ирландского сеттера, веймарской легавой; отсутствие С3 компонента комплемента у бретонского эпаньоля; нарушение функции естественных киллерных клеток у бультерьера; снижение общего количества В- и Т-лимфоцитов, нарушение общего количества и соотношения хелперных и цитотоксических Т-лимфоцитов при глубокой пиодермии немецких овчарок.
Первичные иммунные нарушения могут и не зависеть от породных признаков. К такому примеру, присущему для многих пород собак, можно отнести низкий уровень продукции иммуноглобулинов классов IgA и IgM.
Наиболее часто встречающиеся нозологические формы при пиодермиях у собак
Бактериальное воспаление кожи собак, в зависимости от глубины проникновения процесса, принято разделять на поверхностные и глубокие пиодермии.
Поверхностные пиодермии включают импетиго у молодых собак, пиодермию кожно-слизистых зон, интертриго, а также поверхностный бактериальный фолликулит.
Глубокие пиодермии в ряду нозологий содержат глубокий фолликулит, фурункулез, воспаление подкожной клетчатки, пиотравматический фолликулит и фурункулез, назальный фолликулит и фурункулез, фолликулит и фурункулез области морды (акне).
Нозологические формы пиодермии.
Клинические симптомы
В большинстве случаев холецистит наблюдается как острое заболевание. Владельцы отмечают у животного тошноту, рвоту, отказ от корма, боли в области живота. Желтуха является необязательным симптомом, особенно если общий желчный проток свободен, и может проявляться не сразу. Ее появление в этом случае объясняется развитием неспецифического реактивного гепатита и внутрипеченочного холестаза в ответ на эндотоксины из воспаленного желчного пузыря. Холецистит, сопровождающийся застоем желчи, может приводить к ахолии и обесцвечиванию каловых масс. Появление на фоне этих симптомов лихорадки, синдрома острого живота и признаков септического шока (поверхностное дыхание, гипотермия, бледные десна и слабый, но частый пульс) может указывать на разрыв желчного пузыря и требует неотложных мероприятий.
Холецистит может быть хроническим и проявляться периодической тошнотой у животного, признаками дискомфорта после еды, потерей аппетита, снижением веса, диареей или протекать вообще без каких-либо симптомов (а изменения в желчном пузыре будут случайной находкой при ультрасонографии).
Механизм образования NETs
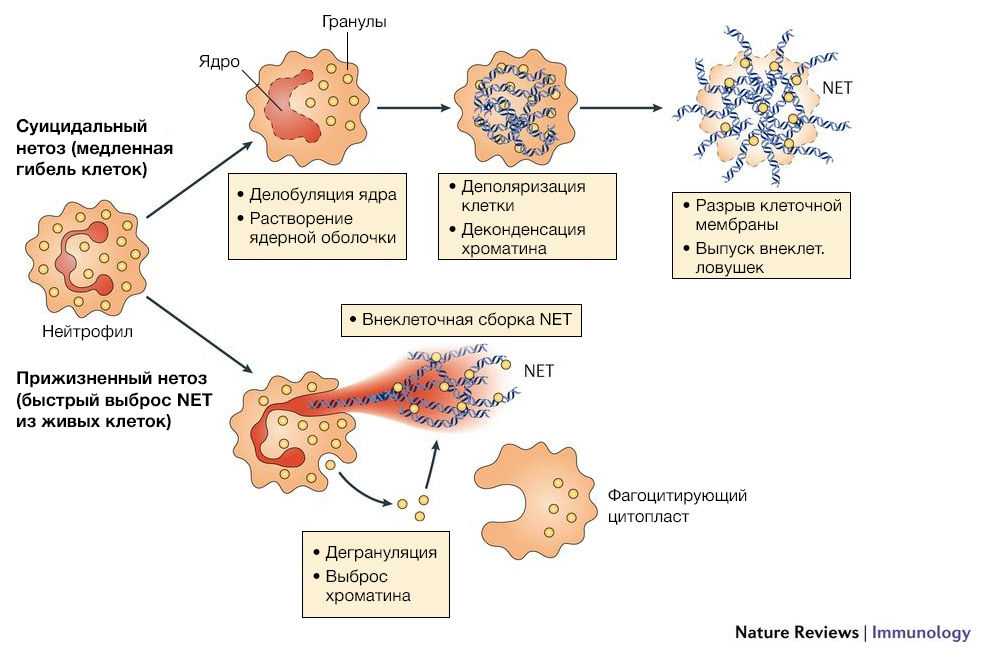
Основными компонентами внеклеточных нейтрофильных ловушек являются гистоны, ферменты и пептиды гранул (нейтрофильная эластаза, миелопероксидаза, катепсин G, лактоферрин, желатиназа, лизоцим С, кальпротектин и другие). Процесс образования NETs называется NETosis и может быть вызван различными индукторами: микроорганизмами, бактериальными компонентами, активированными тромбоцитами, комплементарными пептидами, аутоантителами, IL-8, перекисью водорода, кристаллами урата, сигаретным дымом. После контакта индуктора с рецепторами на мембране клетки активируется молекулярный каскад, который приводит к выходу кальция из эндоплазматического ретикулума, что в свою очередь вызывает повышение активности цитоплазматической деиминазы PAD4. Наряду с этим уменьшается конденсация хроматина. Через некоторое время нейтрофилы теряют гетерохроматические области ядра, в результате чего ядра расширяются и становятся круглыми. Ядерная оболочка распадается на везикулы, мембраны гранул и митохондрий разрушаются, что приводит к смешению цитоплазмы, кариоплазмы и антибактериальных пептидов. Белки гранул адсорбируются на отрицательно заряженных фибриллах деконденсированного хроматина, который служит скелетом для ловушки. В конечном итоге клеточная мембрана разрывается и содержимое клетки выбрасывается наружу и разворачивается в пространстве, образуя сеть .
Описанный механизм называется suicidal NETosis (суицидальный нетоз). Однако известно, что нейтрофилы могут продуцировать NET, выделяя часть ядра или ядро целиком, и не нарушать целостность клеточной мембраны. Такой механизм получил название vital NETosis (прижизненный нетоз). Эти две формы одного и того же процесса имеют существенные различия. Во-первых, суицидальный нетоз вызывается в основном химической стимуляцией гранулоцитов и требует несколько часов для продукции NET, в то время как прижизненный нетоз активируется при раздражении нейтрофилов бактериальными агентами и занимает меньшее время. Во-вторых, vital NETosis не приводит к лизированию клетки, и она сохраняет способность к хемотаксису и фагоцитозу. Третье отличие заключается в механизме выпуска ловушек. Как было описано выше, при суицидальном нетозе происходит деконденсация хроматина, растворение ядерной оболочки и выброс содержимого клетки через перфорацию в плазматической мембране. Во время прижизненного нетоза происходит перенос ДНК из ядра во внеклеточное пространство с помощью везикул. Везикулы с ДНК, отделившиеся от ядра, проходят через цитоплазму и сливаются с клеточной мембраной, тем самым выбрасывая NET из клетки без перфорации мембраны .
Причины
Одной из основных причин являются бактериальные и вирусные инфекции. Ключевую роль в развитии заболевания играют воспалительные процессы, химиотерапия, авитаминоз, травма костного мозга, апластическая анемия и продолжительный прием медикаментозных препаратов (химиотерапия, длительное лечение гормональными препаратами и т.д.). Иногда первопричину заболевания установить достаточно сложно, поэтому оно диагностируется как самостоятельная патология. Однако основной причиной возникновения болезни является снижение активности гранулоцитов, что вызвано их разрушением в кровотоке, снижением пролиферации (синтеза) клеток-предшественников, стволовых клеток костного мозга и нарушениями на стадии дифференциации протоклеток.
Лечение нейтропении
Классической схемы лечения нейтропении не существует по причине разнообразия симптоматики и причин патологии. Интенсивность терапии зависит от общего состояния пациента, его возраста, характера микрофлоры, вызывающей воспалительный процесс. При инфекционных осложнениях назначаются антибактериальные, противовирусные и противогрибковые средства. Транзиторная нейтропения у больных злокачественными опухолями, вызванная химиотерапией или облучением, требует назначения антибиотиков до момента восстановления минимального уровня нейтрофилов. В последнее время популярность приобретает применение колониестимулирущих фокторов (филграстим) в сочетании с препаратами, улучшающие обменные процессы и регенерацию (метилурацил, пентоксил) или препарата Нуклеоспермат натрия, оказывающего комплексное влияние как на активацию эндогенных колониестимулирующих факторов (КСФ) и клеточного противовирусного и противобактериального иммунитета, так и стимулирование процессов регенерации ткани. Одним из вариантов радикального лечения некоторых наследственных и приобретенных (онкология) форм нейтропении является пересадка донорского костного мозга.
Прежде чем назначить схему лечения, врачу необходимо получить результаты клинических исследований, на основании которых определяется степень тяжести вторичного заболевания.
Что такое нейтрофилы и их функции в организме
Для понимания сути этого воспаления и его нюансов нужно знать, что такое нейтрофилы и каковы их функции в организме собаки, да и любого животного.
Нейтрофилы являются одними из «исполнительных механизмов» иммунной системы животных и человека. Это клетки, максимальный размер которых не превышает 9–12 мкм. Синтезируются и вызревают в красном костном мозге.
Если говорить по-научному, то нейтрофилы – разновидность лейкоцитов гранулоцитарного типа. «Нейтрофилами» их назвали оттого, что эти клетки одинаково хорошо прокрашиваются всеми видами основных красителей, используемых в гематологии при микроскопическом исследовании крови.
Такое название они получили оттого, что в цитоплазме этих клеток имеются особые зернистые включения
Мы не случайно акцентируем внимание на цитоплазме. У нейтрофилов в ней содержится огромное количество «жестких» ферментных комплексов, за счет которых, собственно, эти клетки могут выполнять свои функции в организме животных и человека
Если конкретнее, то за счет агрессивных типов ферментов они могут растворять те элементы, наличие которых в здоровом организме не предполагается.
Последнее обстоятельство связано с тем, что нейтрофилы занимаются в основном фагоцитозом (т.е. поглощают, «проглатывают» микробов). Но, в силу своих размеров, справиться с большими объектами они физически не в состоянии. Кроме того, эти клетки являются своеобразными «смертниками», так как после акта фагоцитоза они обычно погибают. Их гибель, однако, не является бесполезной: оболочка нейтрофила разрушается и на «волю» высвобождаются ферментные комплексы.
Именно здесь кроется основная особенность нейтрофилов. Погибшие клетки и их ферменты смешиваются с болезнетворными микроорганизмами, начиная растворять их в однородную массу. Последняя известна всем: это не что иное, как гной. Так что именно нейтрофилы «ответственны» за гнойный тип воспаления. Так что живут эти маленькие защитники недолго: если в организме есть очаги воспаления, срок их жизни редко превышает пару дней.
Впрочем, есть у нейтрофилов и другая важная задача. Они оставляют в очаге будущего воспаления химические маркеры, своеобразные «маяки», называемые «хемокины». Ориентируясь на них, на помощь прибывают иные типы клеток иммунной системы.






